COVID-19 được WHO tuyên bố là đại dịch toàn cầu đã ảnh hưởng đến hàng triệu bệnh nhân trên khắp thế giới. COVID-19 ảnh hưởng không cân đối đến những người có mắc các bệnh lý nội tiết, do đó làm tăng nguy cơ mắc bệnh lý nặng nề, nghiêm trọng. Chúng tôi sẽ thảo luận về các cơ chế khiến những người có vấn đề về nội tiết có dễ mắc COVID-19 nặng dựa trên các bằng chứng khoa học. Chúng tôi cũng đề xuất các biện pháp phòng ngừa và quản lý các bệnh lý nội tiết trong bối cảnh lệnh giới nghiêm toàn cầu đang được áp dụng và đưa ra các lời khuyên thiết thực để việc chăm sóc các bệnh nhân có bệnh lý nội tiết không bị gián đoạn.
Từ khóa: COVID-19, nội tiết, đái tháo đường, tăng huyết áp, béo phì, hội chứng chuyển hóa.
Bệnh do Coronavirus 2019 (COVID-19) được Tổ chức Y tế Thế giới (WHO) tuyên bố là đại dịch vào ngày 11 tháng 3 năm 2020 với hơn 3.059.642 trường hợp mắc và 211.028 trường hợp tử vong được báo cáo từ 213 quốc gia và vùng lãnh thổ tại thời điểm viết bài này. Ngày càng có nhiều bằng chứng cho thấy rằng những bệnh nhân mắc các bệnh nội tiết như đái tháo đường (ĐTĐ), tăng huyết áp (THA), béo phì và bệnh lý tim mạch có nguy cơ mắc các biến chứng liên quan đến COVID-19 cao hơn. Các báo cáo từ Anh và Mỹ đã chỉ ra tỷ lệ lớn bệnh nhân mắc bệnh ĐTĐ và béo phì nằm trong nhóm những người tử vong vì COVID-19 và những trường hợp mắc COVID-19 nặng. Ở Mỹ, các bệnh kèm theo chuyển hóa tim mạch phổ biến nhất liên quan đến COVID-19 là THA (49,7%), béo phì (48,3%), ĐTĐ (28,3%) và bệnh tim mạch (27,8%) (Hình 1). Hơn nữa, ĐTĐ là bệnh đi kèm phổ biến nhất trong các ca tử vong do COVID-19 theo một báo cáo khác. Với những dữ liệu này, cả WHO và Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Hoa Kỳ (CDC) đều liệt kê ĐTĐ, THA và béo phì là các yếu tố nguy cơ dẫn đến các biến chứng COVID-19 nghiêm trọng hơn. Trong bài tổng quan này, chúng tôi tóm tắt các bệnh lý nội tiết phổ biến liên quan đến COVID-19.
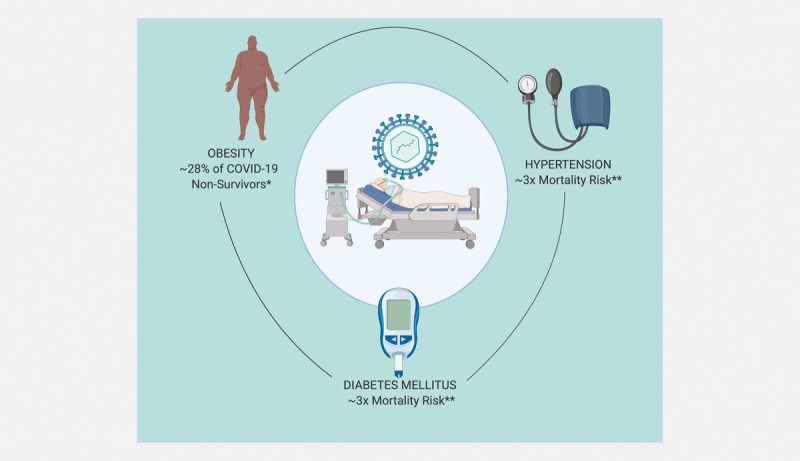 Hình 1: Tác động lâm sàng của các bệnh lý nội tiết đối với COVID-19 (Cập nhật từ Bộ Y tế Louisiana ngày 27/3/2020. http://ldh.la.gov ** tài liệu tham khảo 3)
Hình 1: Tác động lâm sàng của các bệnh lý nội tiết đối với COVID-19 (Cập nhật từ Bộ Y tế Louisiana ngày 27/3/2020. http://ldh.la.gov ** tài liệu tham khảo 3)
Hội chứng suy hô hấp cấp tính nặng do coronavirus-2 gây ra (SARS-CoV-2) là một loại betacoronavirus được xác định là tác nhân gây bệnh COVID-19. Virus này xâm nhập vào môi trường nội bào bằng cách liên kết protein gai trên vùng liên kết thụ thể của nó (RBD) với enzyme chuyển đổi angiotensin II (ACE2) có trên bề mặt biểu mô của tế bào người (Hình 2). Đáng chú ý, ACE2 là một phân tử phân biệt từ enzym chuyển đổi angiotensin I (ACE1), là một mục tiêu điều trị. Sau khi gắn vào ACE2, SARS-CoV-2 thu nạp thêm một serine protease TMPRSS2, tạo điều kiện thuận lợi cho virus xâm nhập vào tế bào chất (Hình 2). ACE2 sau đó bị phân cắt bởi một enzyme là ADAMTS17 protease, do đó làm giảm biểu hiện trên bề mặt tế bào. Sau khi xâm nhập vào tế bào chất, virus xâm nhập vào nhân qua con đường nội bào và quá trình nhân lên của virus diễn ra sau đó.
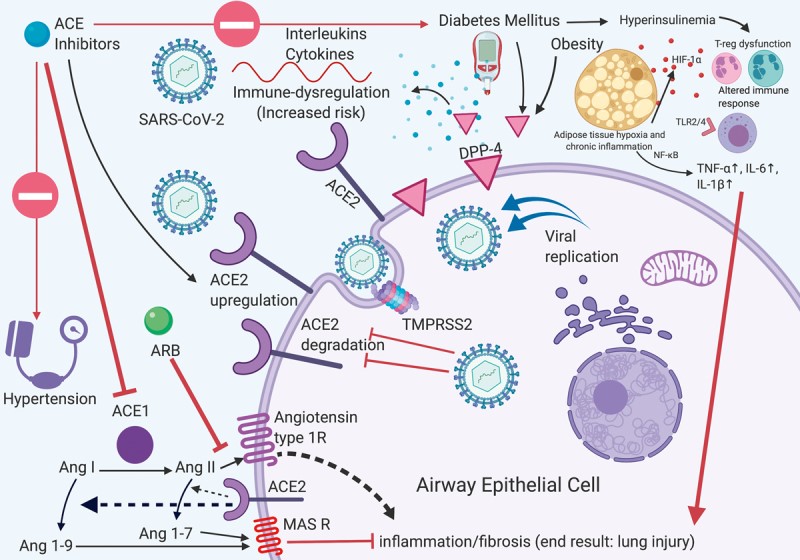 Hình 2: Tác động qua lại giữa các phân tử trong các bệnh lý nội tiết, sự biến đổi ACE và COVID-19: Minh họa các bệnh lý nội tiết, các yếu tố giảm nhẹ và các nguy cơ liên quan của COVID-19. Mũi tên đỏ thể hiện tác dụng có hại, mũi tên chặn phản ánh sự ức chế. ACE: Men chuyển đổi angiotensin; ARB: Thuốc chẹn thụ thể angiotensin; Ang: Angiotensin; DPP-4: Dipeptidyl peptidase-4.
Hình 2: Tác động qua lại giữa các phân tử trong các bệnh lý nội tiết, sự biến đổi ACE và COVID-19: Minh họa các bệnh lý nội tiết, các yếu tố giảm nhẹ và các nguy cơ liên quan của COVID-19. Mũi tên đỏ thể hiện tác dụng có hại, mũi tên chặn phản ánh sự ức chế. ACE: Men chuyển đổi angiotensin; ARB: Thuốc chẹn thụ thể angiotensin; Ang: Angiotensin; DPP-4: Dipeptidyl peptidase-4.
Sinh lý bệnh và nguy cơ
Có một số lý do tại sao ĐTĐ lại làm trầm trọng thêm nguy cơ mắc biến chứng COVID-19 nghiêm trọng.
+ Đầu tiên, ĐTĐ có thể tạo điều kiện thuận lợi cho sự xâm nhập vào tế bào của SARS-CoV-2 bằng cách làm tăng biểu hiện bề mặt của ACE2 thông qua giảm hoạt động ADAMTS17 qua trung gian tăng insulin máu. Các nhà nghiên cứu nhận thấy có sự biểu hiện cao hơn của protein ACE2 trong đảo tụy có liên quan đến tính trạng tăng đường huyết và bệnh ĐTĐ do SARS-coronavirus (SARS-CoV) – một loại coronavirus khác sử dụng ACE2 để xâm nhập tế bào, điều đó cho thấy rằng SARS-CoV-2 có thể hoạt động thông qua một cơ chế tương tự.
+ Thứ hai, các chất điều hòa ACE2 như chất ức chế ACE1 (ACEi), thuốc chẹn thụ thể angiotensin (ARB), và thiazolidenedione, được sử dụng thường xuyên trong ĐTĐ có thể điều chỉnh sự biểu hiện của ACE2.
+ Thứ ba, ĐTĐ có liên quan đến khiếm khuyết bổ thể và giảm kháng nguyên kích thích IL-6, IL-8 và TNF-α; và suy giảm tế bào T điều hòa (Tregs) và tế bào trình diện kháng nguyên (APC) nên làm trầm trọng thêm tình trạng suy giảm miễn dịch.
+ Thứ tư, THA và béo phì đồng thời, thông qua HIF-1α và các toll-like receptor, có thể góp phần gây ra tình trạng viêm mãn tính dẫn đến suy giảm khả năng loại bỏ SARS-CoV-2 qua trung gian miễn dịch.
+ Cuối cùng, dipeptidyl peptidase-4 (DPP-4), một glycoprotein bề mặt, phân giải GLP-1 làm tăng khả năng mắc ĐTĐ và béo phì, và cũng có chức năng như một thụ thể bề mặt cho coronavirus. Mặc dù vai trò DPP-4 vẫn chưa được hiểu rõ đối với SARS-CoV-2, vai trò duy nhất của DPP-4 trong nhiễm trùng coronavirus là làm cho việc ức chế DPP-4 trở thành một mục tiêu điều trị khả dĩ, có thể hoạt động bằng cách giảm biểu hiện DPP-4 và bù trừ cytokine qua trung gian tổn thương cơ quan đích. Đánh giá này được củng cố thêm bằng bằng chứng rằng sự ức chế DPP-4 cho thấy tác dụng chống viêm trong các nghiên cứu tiền lâm sàng trên người. Tóm lại, bệnh nhân ĐTĐ có thể dễ mắc cơn bão cytokine dẫn đến tổn thương cơ quan đích và tử vong (Hình 2).
Một đánh giá của mười sáu nghiên cứu lâm sàng với tổng số 9.011 bệnh nhân bị COVID-19 cho thấy tỷ lệ hiện mắc bệnh ĐTĐ từ 2,0% đến 56,6% [trung vị (IQR)%: 13,2 (9,10–23,70)], làm nổi bật nguy cơ cao mà bệnh nhân ĐTĐ đối mặt với đại dịch COVID-19 toàn cầu (Bảng 1). Ngoài ra, tình trạng tăng đường máu đã được thấy ở 35–58% bệnh nhân điệu trị nội trú với COVID-19 cho thấy gánh nặng của rối loạn chuyển hóa glucose. Các nghiên cứu khác đã báo cáo tỷ lệ mắc bệnh ĐTĐ ở các trường hợp nặng do COVID-19 so với các trường hợp nhẹ (14,3% so với 5,0%, p = 0,009), cũng như tăng nguy cơ tử vong và tăng tỷ lệ tử vong ở bệnh nhân ĐTĐ (~ 3x, Hình 1 ), so với bệnh nhân không mắc ĐTĐ (tương ứng là 7,3% so với 2,3%). Trong một nghiên cứu khác, ĐTĐ được đánh dấu là bệnh đi kèm phổ biến nhất xảy ra ở 41% tổng số ca tử vong do COVID-19. Ngoài ra, một nghiên cứu ghi nhận rằng những bệnh nhân đồng thời mắc ĐTĐ và COVID-19 có tỷ lệ tử vong là 16,5% so với 0% ở những bệnh nhân COVID-19 không mắc bệnh đi kèm, trong khi một nghiên cứu khác báo cáo kết quả kém ở bệnh nhân nội trú COVID-19 bị tăng đường huyết không kiểm soát được so với đối với các đối tác euglycemic của họ. CDC Hoa Kỳ đã liệt kê ĐTĐ vào một trong các yếu tố nguy cơ của COVID-19 nghiêm trọng trong hướng dẫn lâm sàng.
Bảng 1 Tỷ lệ mắc bệnh đái tháo đường (ĐTĐ) và tăng huyết áp (THA) ở bệnh nhân COVID-19.
| Tiêu đề | Tác giả | Mẫu | Tỷ lệ mắc ĐTĐ | Tỷ lệ THA | Tỷ lệ béo phì |
| Clinical Course and Outcomes of Critically Ill Patients With SARS-CoV-2 Pneumonia in Wuhan, China: A Single-Centered, Retrospective, Observational Study | Yang et al. 29 | 52 critically sick patients | 17% | NR | NR |
| Clinical Characteristics of Coronavirus Disease 2019 in China | Guan et al. 82 | 1099 patients | 7.40% | 15% | NR |
| Clinical characteristics of 140 patients infected with SARS-CoV-2 in Wuhan, China | Zhang et al. 31 | 140 patients | 12.10% | 30% | NR |
| Clinical Characteristics of 138 Hospitalized Patients With 2019 Novel Coronavirus-Infected Pneumonia in Wuhan, China | Wang et al. 32 | 138 patients | 10.10% | 31.20% | NR |
| Clinical findings in a group of patients infected with the 2019 novel coronavirus (SARS-Cov-2) outside of Wuhan, China: retrospective case series | Xu et al. 33 | 62 patients | 2% | 8% | NR |
| Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study | Chen et al. 34 | 99 patients | 13% | NR | NR |
| A familial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster | Chan et al. 41 | Family of 6 patients | 16% | 32% | NR |
| Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study | Zhou et al. 3 | 191 patients | 19% | 30% | NR |
| Analysis of Myocardial Injury and Cardiovascular Diseases in Critical Patients with New Coronavirus Pneumonia | Chen et al. 83 | 150 patients | 13.3% | 32.6% | NR |
| A Trial of Lopinavir-Ritonavir in Adults Hospitalized with Severe Covid-19 | Cao et al. 36 | 199 patients | 11.16% | NR | NR |
| Characteristics and Outcomes of 21 Critically Ill Patients With COVID-19 in Washington State | Arentz et al. 38 | 21 critically sick patients | 33.3% | NR | NR |
| Epidemiologic and Clinical Characteristics of 91 Hospitalized Patients with COVID-19 in Zhejiang, China: A retrospective, multi-centre case series. | Qian et al. 40 | 91 patients | 8.79% | 16.48% | NR |
| Host susceptibility to severe COVID-19 and establishment of a host risk score: findings of 487 cases outside Wuhan. | Shi et al. 39 | 487 patients | 6% | 20.3% | NR |
| Clinical Characteristics of Covid-19 in New York City | Goyal et al. 42 | 393 patients | 25.2% | 50.1% | 35.8% |
| Hospitalization Rates and Characteristics of Patients Hospitalized with Laboratory-Confirmed Coronavirus Disease 2019 — COVID-NET, 14 States, March 1–30, 2020 | Garg et al. 6 | 178 patients | 28.3% | 49.7% | 48.3% |
| Presenting Characteristics, Comorbidities, and Outcomes Among 5700 Patients Hospitalized With COVID-19 in the New York City Area | Richardson et al. 43 | 5700 patients | 56.6% | 33.8% | 41.7% |
NR: Not reported (chưa được báo cáo).
Bằng chứng về sự gia tăng nguy cơ biến chứng chuyển hóa lâu dài ở những bệnh nhân đã khỏi suy hô hấp cấp do SARS-CoV gây ra, làm dấy lên lo ngại về nguy cơ có thể xảy ra các biến chứng tương tự ở những người mắc COVID-19. Điều này đã được chứng minh trong một nghiên cứu trên 31 bệnh nhân SARS đã hồi phục so với những người tình nguyện khỏe mạnh ở tuổi 12 cho thấy chuyển hóa glucose bất thường ở 60% (so với 16%), tăng lipid máu ở 68% (so với 40%), và bất thường tim mạch ở 44% (so với 0%) những người tham gia nghiên cứu. Người ta giả thiết rằng việc sử dụng glucocorticoid tĩnh mạch ở liều cao trong thời gian ngắn có thể đã góp phần gây ra những rối loạn chuyển hóa lâu dài này. Sử dụng glucocorticoid ở bệnh nhân COVID-19 nhập viện cũng có thể đóng một vai trò trong việc tăng đường huyết cấp tính ở những bệnh nhân này. Tuy nhiên, việc sử dụng glucocorticoid đã không còn được ưa chuộng trong việc điều trị thường quy COVID-19 theo hướng dẫn của CDC và WHO và bằng chứng cho thấy glucocorticoid làm giảm nồng độ angiotensin chống viêm 1-7 và làm chậm quá trình loại bỏ virus (Hình 3), cung cấp cơ sở phân tử để tránh sử dụng trên toàn cầu. Một thử nghiệm lâm sàng hiện đang được tiến hành để xác định hiệu quả của liệu pháp glucocorticoid toàn thân trong COVID-19.
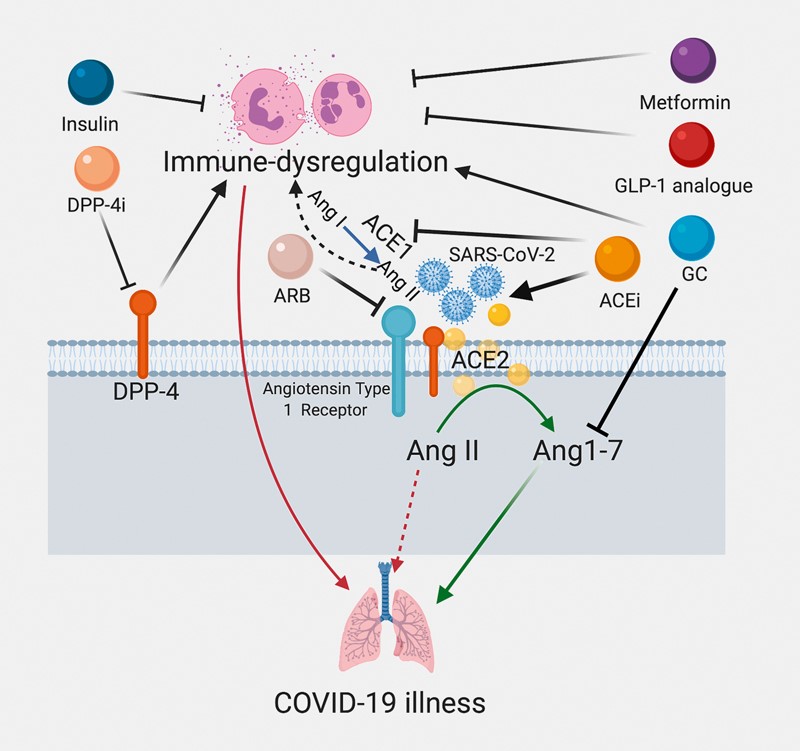 Hình 3: Ảnh hưởng của các thuốc thường dùng trong bệnh béo phì, đái tháo đường và tăng huyết áp đối với sự điều hòa miễn dịch. Mũi tên màu đỏ cho biết tác động tiêu cực, mũi tên màu xanh lá cây cho biết tác động tích cực, mũi tên màu đen phản ánh kích thích và mũi tên chặn biểu thị sự ức chế. ACE: Men chuyển đổi angiotensin; ARB: Thuốc chẹn thụ thể angiotensin; Ang: Angiotensin; DPP-4: Dipeptidyl peptidase-4; GLP-1: Glucagon như peptit-1; GC: Glucocorticoid.
Hình 3: Ảnh hưởng của các thuốc thường dùng trong bệnh béo phì, đái tháo đường và tăng huyết áp đối với sự điều hòa miễn dịch. Mũi tên màu đỏ cho biết tác động tiêu cực, mũi tên màu xanh lá cây cho biết tác động tích cực, mũi tên màu đen phản ánh kích thích và mũi tên chặn biểu thị sự ức chế. ACE: Men chuyển đổi angiotensin; ARB: Thuốc chẹn thụ thể angiotensin; Ang: Angiotensin; DPP-4: Dipeptidyl peptidase-4; GLP-1: Glucagon như peptit-1; GC: Glucocorticoid.
Tiếp cận lâm sàng
Gần đây, Hiệp hội Đái tháo đường Hoa Kỳ (ADA) đã đưa ra các khuyến cáo cho bệnh nhân về việc chuẩn bị và dự phòng đối với COVID-19 (bảng 2) bao gồm cả việc cập nhật thông tin liên hệ; đảm bảo dự trữ đầy đủ carbohydrate đơn giản, thuốc và insulin; và đảm bảo có sẵn các nguồn cung cấp như cồn tẩy rửa, bộ kits glucagon, que thử ketone, xà phòng và các vật dụng gia đình. Hiệp hội các nhà nội tiết lâm sàng Hoa Kỳ cũng nhấn mạnh sự chuẩn bị sẵn sàng khẩn cấp đầy đủ và cung cấp checklist các hạng mục hành động trong kế hoạch khẩn cấp để đảm bảo việc chăm sóc bệnh nhân ĐTĐ không bị gián đoạn (bảng 2).
Bảng 2 Nội tiết và COVID-19: Nguồn và Link.
| Tổ chức | Nguồn | Web Link |
| American Association of Clinical Endocrinologists | Diabetes emergency plan (for patients) | http://mydiabetesemergencyplan.com |
| Endocrine Society | General resources for endocrinologists | https://www.endocrine.org |
| European Society of Endocrinology | General resources for endocrinologists | https://www.ese-hormones.org |
| Society for Endocrinology | General resources for endocrinologists | https://www.endocrinology.org/clinical-practice/covid-19-resources-formanaging- endocrine-conditions |
| Society for Endocrinology | Adrenal insufficiency positionstatement | https://www.endocrinology.org/news/item/14050/Coronavirus-advicestatement- for-patients-with-adrenal %2fpituitary-insufficiency |
| American Diabetes Association | Inpatient blood glucose management | https://care.diabetesjournals.org/content/43/Supplement_1/S193 |
| American Thyroid Association | Frequently asked questions | https://www.thyroid.org/covid-19/coronavirus-frequently-asked-questions |
| National Osteoporosis Foundation | Patients and Providers Fact Sheet | https://cdn.nof.org/wp-content/uploads/NOF-COVID-Factsheet_.pdf |
| National Center for Transgender Equality | Plan of Action | https://transequality.org/covid19/plan |
| The National Institute of Diabetes and Digestive and Kidney Diseases | General guidelines | https://www.niddk.nih.gov/health-information/endocrine-diseases/adrenalinsufficiency- addisons-disease |
| Centers for Disease Control and Prevention | General guidelines | https://www.cdc.gov/coronavirus/2019-ncov/index.html |
| World Health Organization | General guidelines | https://www.who.int/emergencies/diseases/novel-coronavirus-2019 |
Từ quan điểm thực hành lâm sàng, việc tư vấn cho bệnh nhân nên bao gồm thảo luận về các mục tiêu đường huyết và chế độ dùng insulin trong những ngày ốm, cũng như cung cấp đủ nước và thức ăn (bao gồm cả những đồ ăn lâu hư, glucose và điện giải). Hơn nữa, nên khuyến khích việc áp dụng và tiếp tục chế độ ăn uống lành mạnh và tập thể dục 150 phút hàng tuần như đi bộ trong nhà và các bài tập phù hợp về thể chất khác. Nên nhấn mạnh việc tiêm chủng đối với bệnh cúm, phế cầu và các bệnh nhiễm trùng khác (dựa trên CDC hoặc hướng dẫn của chính quyền địa phương tương đương). Yếu tố thứ hai có tầm quan trọng lớn vì tình trạng đồng nhiễm virus đã xảy ra thường xuyên trong COVID-19. Hơn nữa, bệnh nhân nên được thông báo về tình trạng có thể mua insulin mà không cần theo đơn thuốc ở nhiều quốc gia như một biện pháp dự phòng (Mỹ, Canada, Ấn Độ, Mexico, v.v.)
Để quản lý tăng đường huyết cho bệnh nhân nội trú, mục tiêu đường huyết được khuyến nghị bởi ADA là 140–180 mg/dL cho hầu hết các bệnh nhân bị bệnh nặng và không nghiêm trọng, đối với những bệnh nhân được lựa chọn có khả năng phòng tránh tốt hạ đường huyết thì mục tiêu đường huyết nghiêm ngặt hơn (đường huyết 110–140 mg/dL). Tuy nhiên, cho đến nay, ADA vẫn chưa đưa ra các mục tiêu cụ thể về đường huyết cho bệnh nhân có COVID-19. Trong các hướng dẫn nói trên, ADA khuyến nghị xem xét các mục tiêu đường huyết rộng hơn (glucose máu > 180 mg/dL) cho những bệnh nhân mắc bệnh đi kèm nặng, bệnh nan y hoặc không thể theo dõi đường huyết thường xuyên. Ở những bệnh nhân này, các chế độ insulin ít linh hoạt hơn với mục đích giảm thiểu đường niệu, mất nước và rối loạn điện giải có thể thích hợp hơn, tuy nhiên, đánh giá lâm sàng kết hợp với đánh giá liên tục tình trạng lâm sàng bao gồm những thay đổi trong nồng độ glucose, mức độ bệnh, tình trạng dinh dưỡng, hoặc các loại thuốc dùng đồng thời có thể ảnh hưởng đến mức đường huyết, nên được đưa vào quá trình đưa ra quyết định y khoa.
Hơn nữa, việc ngừng sử dụng các chất ức chế đồng vận chuyển natri-glucose-2 (SGLT-2i) là hợp lý vì điều đó có liên quan đến suy giảm thể tích nội mạch và tăng nguy cơ nhiễm ceton huyết. Việc ngừng sử dụng sulfonylurea cũng được khuyến khích, đặc biệt ở những bệnh nhân nguy kịch, nơi mà độ thanh thải qua thận của thuốc có thể bị ảnh hưởng. Chloroquine và hydroxochloroquine, đang được nghiên cứu về hiệu quả trong điều trị COVID-19, có thể gây hạ đường huyết. Ngược lại, các loại thuốc kháng virus như ritonavir và lopinavir, đã được sử dụng cho COVID-19 trước đây, có liên quan đến tăng đường huyết. Việc sử dụng các thuốc này cũng nên đi kèm với việc điều chỉnh phác đồ điều trị bệnh ĐTĐ.
Do nhu cầu quản lý linh hoạt, insulin vẫn là loại thuốc an toàn nhất để kiểm soát tăng đường huyết ở bệnh nhân ĐTĐ và có thêm tác dụng chống viêm trong tình trạng bệnh nặng. Điều quan trọng là, các chất ức chế DPP-4 và các chất tương tự thụ thể GLP-1 có thể không chỉ làm giảm tình trạng viêm mãn tính trong ĐTĐ mà còn có tác dụng bảo vệ phổi và điều hòa miễn dịch (trong các nghiên cứu tiền lâm sàng) và có thể chứng minh là có lợi (Hình 3).
Việc đầu cơ tích trữ là một mối đe dọa lớn trong cuộc khủng hoảng này. May mắn thay, cho đến nay, không có báo cáo nào về tình trạng thiếu hụt nguồn cung cấp y tế và bác sĩ lâm sàng nên khuyên bệnh nhân chống lại điều này để đảm bảo cung cấp đủ cho những người khác.
Nguồn lực và hướng đi trong tương lai
Hiệp hội Nội tiết đã thành lập một trang web COVID-19 chuyên dụng với cá c nguồntài nguyên dành cho các bác sĩ và nhà nghiên cứu thuộc nhiều hiệp hội khác như Hiệp hội Nội tiết Châu Âu và Hiệp hội Nội tiết (bảng 2).
Đại dịch này đã dẫn đến sự phát triển nhanh chóng của y học từ xa. Các nhà chức trách ở Hoa Kỳ, Canada và Pháp đã công bố phạm vi phủ sóng rộng hơn của các cuộc khám bệnh từ xa, có khả năng mang lại lợi ích trực tiếp cho bệnh nhân ĐTĐ. Tuy nhiên, người ta không biết liệu các cuộc thăm khám bằng y tế từ xa có đủ để theo dõi việc tiêm insulin hay không, vốn hiện nay bắt buộc phải thăm khám tại chỗ.
Vẫn còn nhiều điểm chưa chắc chắn cần được kiểm tra thêm về ĐTĐ và COVID-19. Một số trong số này bao gồm sự khác biệt giữa ĐTĐ típ 1 và típ 2, kiểm soát đường huyết tối ưu so với kiểm soát đường huyết kém, và ảnh hưởng của tuổi tác và các tình trạng đồng thời khác ở bệnh nhân ĐTĐ trong số những bệnh nhân khác.
Sinh lý bệnh và nguy cơ
Tỷ lệ THA (Tăng huyết áp) cao đã được ghi nhận ở những bệnh nhân bị COVID-19, THA có thể dẫn đến nguy cơ cao mắc bệnh nặng hơn. Nguy cơ có thể xuất phát từ nhiều lý do. Trước hết, THA có liên quan đến rối loạn điều hòa miễn dịch, biểu hiện là mức IL-17 cao hơn, chức năng tế bào NK bất thường và sự bất thường tế bào T gây độc tế bào (Tc) có thể đảo lộn một phần với các chất đối kháng mineralocorticoid receptor. Các yếu tố góp phần khác bao gồm hoạt hóa giao cảm quá mức, rối loạn điều hòa NFκB và sự gia tăng peptide tiền viêm, angiotensin II (Hình 2).
Một đánh giá của mười hai nghiên cứu, bao gồm dữ liệu từ 8.635 bệnh nhân với COVID-19, cho thấy tỷ lệ mắc THA là từ 8,0 đến 50,1% [trung bình (IQR)%: 30,6 (17,43–33,50)] ( Bảng 1 ). Một nghiên cứu tại Hoa Kỳ đã báo cáo tỷ lệ phổ biến THA là 50,1% . Hơn nữa, một nghiên cứu trên 191 bệnh nhân cho thấy nguy cơ tử vong cao gấp 3 lần ở bệnh nhân THA trong khi các nghiên cứu khác cho thấy nguy cơ mắc COVID-19 nặng gấp 1,57–2,71 lần ( Hình 1 ). Shi và cộng sự. cũng đề cập THA là một trong ba chỉ số trong thang điểm đánh giá nguy cơ COVID-19. Nguy cơ này có thể tăng cao hơn nữa bởi sự đồng mắc của ĐTĐ, hiện diện ở 60,2–85,8% những người bị THA (tùy thuộc vào ngưỡng chẩn đoán được sử dụng).
Tuy nhiên, cần lưu ý rằng THA rất phổ biến ở người cao tuổi và người cao tuổi lại chiếm đa số trong số bệnh nhân COVID-19 cần nhập viện và chăm sóc nguy kịch. Do đó, rủi ro do THA gây ra có thể là kết quả của quan hệ nhân quả nghịch. Tỷ lệ THA hoặc ĐTĐ có thể cao hơn ở những bệnh nhân nặng, nhưng các nghiên cứu đã không báo cáo được nếu những bệnh đi kèm này cùng tồn tại ở những người khác, do đó làm tăng nguy cơ mắc bệnh trầm trọng. Sự cô lập toàn diện về mắc ĐTĐ hoặc ĐTĐ chưa được báo cáo. Do đó, rủi ro nhân quả do những bệnh đi kèm này mang lại riêng lẻ, hoặc cùng nhau, chưa được xác định và vẫn chưa rõ ràng.
Hệ renin-angiotensin-aldosterone và COVID-19
SARS-CoV-2 xâm nhập vào cơ thể người thông qua việc gắn vào các thụ thể ACE2 có trên bề mặt tế bào của tế bào biểu mô phế nang loại 2 trong phổi ( Hình 2 ). Các thụ thể này cũng có trong các mô khác, nồng độ ACE2 trong mô không phải lúc nào cũng tương quan với hoạt động của ACE2 trong huyết tương. Mặc dù ACEi / ARB không ảnh hưởng trực tiếp đến hoạt động của ACE2, một số nghiên cứu trên mô hình động vật thực nghiệm đã chỉ ra rằng ACEi / ARB có thể điều hòa sự biểu hiện và hoạt động của ACE2 trong một số mô nhất định bao gồm cả tim và thận, nhưng các nghiên cứu về tác động của chúng đối với hoạt động và biểu hiện của ACE2 ở phổi bị thiếu. Một nghiên cứu đã chứng minh nồng độ mARN đường ruột của ACE2 tăng lên ở những bệnh nhân được điều trị bằng ACEi trước đây nhưng không tăng ở những người được điều trị bằng ARB. Tương tự, có báo cáo về nồng độ ACE2 trong nước tiểu cao hơn ở bệnh nhân ĐTĐ típ 1,2 nhưng ý nghĩa lâm sàng của những phát hiện này vẫn chưa rõ ràng trong bối cảnh của COVID-19. Dựa trên những phát hiện này, người ta đã đề xuất rằng ACEi / ARB có thể làm tăng nguy cơ mắc COVID-19 nặng và việc đánh giá lại việc sử dụng chúng đã được đề xuất. Ngược lại, ACE2 trong huyết tương cao hơn có thể liên kết với SARS-CoV-2 và bảo vệ chống lại tổn thương phổi và các mô khác (thể hiện trên mô hình động vật) và đây được đề xuất là mục tiêu điều trị. Hơn nữa, angiotensin 1-7 được bổ sung bằng cách sử dụng ACEi / ARB có thể bảo vệ miễn dịch và làm giảm mức độ nặng của COVID-19 bằng cách tác động qua con đường Mas receptor ( Hình 2 ). Tương tự, ACEi có thể làm giảm nồng độ angiotensin II và làm giảm sự điều hòa miễn dịch. Quan điểm này được hỗ trợ thêm bởi các đánh giá gần đây khác chỉ ra bản chất khó hiểu của những khẳng định chưa được chứng minh này liên quan đến nguy cơ cao hơn đối với bệnh nhân COVID-19 dùng ACEi / ARBs. Không có bằng chứng trực tiếp nào chứng minh nguy cơ lý thuyết của việc sử dụng ACEi / ARB liên quan đến mức độ nghiêm trọng của COVID-19 đã được công bố kể từ ngày 22 tháng 4 năm 2020. Một nghiên cứu lâm sàng báo cáo khả năng mắc COVID-19 nhẹ hơn, cải thiện chức năng miễn dịch và giảm tải lượng virus ở bệnh nhân THA được điều trị bằng ACEi / ARB so với những người không được điều trị và kết quả lâm sàng tốt hơn trong một nghiên cứu khác. Những phát hiện này bác bỏ những lo ngại về mặt lý thuyết về các tác nhân này và ủng hộ việc tiếp tục sử dụng ( ban 2 ).
Nhiều tổ chức đã tán thành việc tiếp tục sử dụng ACEi / ARB dựa trên việc thiếu bằng chứng về tác hại ( bảng 2 ). Hiệp hội Tim mạch Châu Âu đã đưa ra khuyến cáo mạnh mẽ “ bệnh nhân và bác sĩ tiếp tục liệu pháp chống tăng huyết áp thông thường vì không có bằng chứng lâm sàng hoặc khoa học cho thấy nên ngừng điều trị bằng ACEi hoặc ARB do nhiễm Covid-19 ”. Nhiều tổ chức khác cũng đã tuyên bố như vậy ( bảng 2 ). Hiệp hội Tim mạch Hoa Kỳ gần đây đã công bố báo cáo việc thiếu các nghiên cứu điều tra và chứng minh bằng chứng về tác hại. Một thử nghiệm lâm sàng: “Enzyme chuyển đổi Angiotensin 2 tái tổ hợp ở người (rhACE2) như một phương pháp điều trị cho bệnh nhân mắc COVID-19” (ClinicalTrials.gov Identifier : NCT04287686 ), hiện đang kiểm tra vai trò của điều hòa thụ thể ACE2 trong COVID-19 và có thể đưa ra kết luận bằng chứng về vấn đề này.
Sinh lý bệnh và nguy cơ
Béo phì gây nên tình trạng thiếu oxy mô mỡ mãn tính dẫn đến trạng thái tiền viêm với mức độ IL-1, IL-6 và TNF-α tăng lên ( Hình 2 và 3 ). Rối loạn chức năng miễn dịch trong béo phì cũng có thể xuất phát từ tình trạng đề kháng insulin của tế bào T. Chúng tôi suy đoán rằng điều này có lẽ sẽ dẫn đến phản ứng miễn dịch bị thay đổi, không chỉ đối với virus mà còn đối với vaccine trong tương lai. Một đánh giá đã nêu ra khả năng mô mỡ như là đích và ổ chứa SARS-CoV-2, mặc dù chưa có nghiên cứu nào phản ánh điều này được công bố cho đến nay. Một nghiên cứu khác đã chứng minh sự lây lan virus influenza kéo dài ở những người béo phì. Tương tự như vậy, sự thay đổi các phản ứng của dòng tủy và lympho trong mô mỡ do đó dẫn đến sự sai lệch của cấu trúc adipokine. Tương tự, béo phì có liên quan tuyến tính với việc tăng mức protein phản ứng C (CRP), được kích hoạt bằng IL-6 có nguồn gốc từ tế bào mỡ . Không có gì ngạc nhiên khi CRP có tương quan với mức độ nặng của bệnh, tạo ra mối liên hệ sinh lý bệnh giữa béo phì và kết quả điều trị COVID-19 kém. Cũng có bằng chứng cho thấy tín hiệu Mas receptor bị suy giảm (của angiotensin 1-7) trong hệ thống renin-angiotensin-aldosterone có thể làm trầm trọng thêm tình trạng rối loạn điều hòa miễn dịch đã có từ trước. Ngoài ra, mức độ DPP-4 tiền viêm cao hơn được thấy ở bệnh béo phì và hậu quả là tăng insulin máu có thể làm trầm trọng thêm nguy cơ COVID-19 một cách độc lập ( Hình 2 và 3 ). Mặc dù lợi ích của việc ức chế DPP-4 chưa được chứng minh, nhưng có tác dụng chống viêm và bảo vệ phổi rõ ràng của các chất tương tự thụ thể GLP-1 trong bệnh béo phì có thể tỏ ra hữu ích trong việc giảm thiểu rủi ro đối với bệnh nặng. Hơn nữa, hội chứng giảm thông khí do béo phì và chứng ngưng thở khi ngủ đồng thời tồn tại, cả hai biến chứng của béo phì, có thể ảnh hưởng đến chức năng hô hấp cũng có thể là nguyên nhân dẫn đến các tác động quan sát được. Hơn nữa, béo phì có liên quan độc lập với nguy cơ huyết khối cao hơn, đặc biệt COVID-19 làm tăng khả năng bệnh vi mạch và huyết khối tĩnh mạch. Sau cùng, kết hợp với tim phổi tổn thương, có thể cản trở nghiêm trọng việc thở máy ở những người béo phì bị bệnh nặng. Hơn nữa, điều quan trọng đối với các nghiên cứu trong tương lai là phân tích mối liên hệ giữa các đặc điểm nhân trắc học của bệnh nhân và COVID-19 nghiêm trọng vì u mỡ nội tạng có khả năng gây nguy cơ cao mắc COVID-19. Trên cơ sở mãn tính hơn, béo phì đặt ra một thách thức cả từ quan điểm điều dưỡng và phục hồi chức năng.
Gần đây, Bộ Y tế Louisana đã báo cáo béo phì là bệnh đi kèm phổ biến thứ ba (sau bệnh ĐTĐ và bệnh thận mãn tính) liên quan đến tỷ lệ tử vong, với tỷ lệ 28% ở những người tử vong COVID-19 ( Hình 1 ). Hơn nữa, CDC báo cáo tình trạng béo phì có ở 48,3% tổng số bệnh nhân nhập viện COVID-19. Một đánh giá của ba nghiên cứu lâm sàng, bao gồm tổng số 6.271 bệnh nhân cho thấy béo phì phổ biến ở 35,8–48,3% [trung vị (IQR)%: 41,7 (35,80–48,30)] của bệnh nhân COVID-19 nhập viện ( Bảng 1 ). Một nghiên cứu khác ghi nhận béo phì là một nguy cơ độc lập đối với việc nhập viện điều trị COVID-19. Dịch vụ Y tế Quốc gia ở Anh cũng báo cáo béo phì là một yếu tố nguy cơ gây bệnh nặng và tử vong ở COVID-19. Dựa trên những dữ liệu này, CDC đã cập nhật hướng dẫn của họ để bao gồm BM I> 40 kg/m2 như một yếu tố nguy cơ của mắc COVID-19 8 nặng .
Điều quan trọng là phải xem xét sinh lý bệnh của các bệnh nội tiết thường được mô tả và mức độ nghiêm trọng của COVID-19. Trong phần này, chúng tôi thảo luận về các cơ chế cơ bản hợp lý đối với COVID-19 nghiêm trọng ở những vật chủ có những rối loạn nội tiết này.
Betacoronavirus, bao gồm SARS-CoV-2, xâm nhập vào tế bào người bằng cách liên kết với ACE2 trong các mô khác nhau. Tuy nhiên, các betacoronavirus như MERS-CoV và SARS-CoV cũng lây nhiễm trực tiếp vào các tế bào miễn dịch. Cụ thể, MERS-CoV liên kết với bạch cầu đơn nhân và tế bào đuôi gai và SARS-CoV ảnh hưởng đến tế bào T thông qua các thụ thể DPP-4. Sau khi tiếp xúc với betacoronavirus, bạch cầu đơn nhân, đại thực bào và tế bào đuôi gai giải phóng cytokine tiền viêm IL-6. IL-6 có hai phương thức tín hiệu ( cis và trans ). Cis -signaling xảy ra khi IL-6 gắn vào các thụ thể liên kết màng của nó (mIL-6R) hiện diện trên các tế bào miễn dịch, gây ra sự hoạt hóa của các tế bào con đường miễn dịch khác như tế bào T, tế bào B và tế bào NK và dẫn đến kích hoạt miễn dịch. Sự kích hoạt bệnh lý của tín hiệu này dẫn đến hội chứng giải phóng cytokine (Cytokine release syndrome: CRS). Trans -signaling xảy ra khi IL-6 liên kết với thụ thể hòa tan của nó (SIL-6R) mà hiện diện trong nội mạc mạch máu. Điều này kích hoạt việc giải phóng yếu tố tăng trưởng nội mô mạch máu (VEGF) và protein hóa trị monocyte-1 (MCP-1). Cùng với việc giảm E-cadherin, kết quả là làm tăng tính thấm thành mạch gây ra các hội chứng như CRS, hội chứng suy hô hấp cấp tính (ARDS) và sốc. Cơ chế truyền tín hiệu bệnh lý thứ ba là con đường trans (khác với Trans -signaling), được trung gian bởi sự gắn IL-6 trên tế bào T-helper 17, dẫn đến hậu quả bệnh lý như ARDS.
Các tác nhân ‘xấu’ của rối loạn điều hòa miễn dịch là tăng béo phì, ĐTĐ và THA và có thể là nguyên nhân dẫn đến mức độ nghiêm trọng của bệnh. Ví dụ, mức IL-6 cao hơn đáng kể trong ĐTĐ típ 1 và 2 và tỷ lệ thuận với BMI ở người béo phì. IL-6 có mối quan hệ hai chiều với ĐTĐ vì nó có liên quan đến việc gây ra kháng insulin và rối loạn cân bằng nội môi của glucose. Tế bào T trong ĐTĐ típ 1 nhạy cảm hơn với IL-6 có thể dẫn đến rối loạn điều hòa miễn dịch và gây ra CRS. Trong THA, nồng độ IL-6 cao hơn, có thể là qua trung gian của sự gia tăng nồng độ angiotensin II và aldosterone, trực tiếp kích hoạt tiết IL-6 bởi hệ mạch. Tác dụng này bị ức chế bởi ARB và các chất đối kháng thụ thể mineralocorticoid. CRP tăng cao (do ảnh hưởng của IL-6) giúp dự báo về mức độ nghiêm trọng của COVID-19, và tăng cao trong bệnh béo phì, ĐTĐ và THA. DPP-4, một đồng thụ thể của betacoronavirus cao hơn ở những người bị béo phì và ĐTĐ, và có tác dụng chống viêm độc lập. Cuối cùng, khả năng phát tín hiệu con đường trans bệnh lý của IL-6 trong bệnh béo phì, ĐTĐ và THA do tình trạng rối loạn điều hòa miễn dịch đã có từ trước, và có thể góp phần vào CRS và các hậu quả lâm sàng như ARDS. Tổng hợp lại, các ‘tác nhân xấu’ của rối loạn điều hòa miễn dịch liên quan đến COVID-19 nghiêm trọng rất phổ biến trong bệnh béo phì, ĐTĐ và THA, và có thể gây ra mức độ nghiêm trọng cao hơn được ghi nhận ở các trạng thái này. Hình 3 mô tả dược lý miễn dịch của các bệnh lý nội tiết và COVID-19.
Trục hạ đồi – tuyến yên – tuyến thượng thận
Glucocorticoid có cả tác dụng kích thích miễn dịch và ức chế. Trong giai đoạn đầu của nhiễm virus, glucocorticoid tạo phản ứng miễn dịch chống lại các kháng nguyên lạ. Tuy nhiên, trong giai đoạn tiến triển của nhiễm virus, sự kích hoạt trục dưới đồi – tuyến yên -tuyến thượng thận có thể xảy ra và có thể dẫn đến suy giảm glucocorticoid trong tình trạng bệnh nguy kịch. Do việc sử dụng rộng rãi glucocorticoid và nguy cơ có thể xảy ra đối với bệnh nhân suy tuyến thượng thận (AI), Hiệp hội Nội tiết đã đưa ra một tuyên bố cho thấy thiếu bằng chứng cho thấy nguy cơ mắc COVID-19 cao hơn ở bệnh nhân AI ( bảng 2 ). Hiệp hội cũng củng cố liều lượng glucocorticoid vào lúc ốm đau và các quy tắc về thể chất vì những bệnh nhân này về mặt lý thuyết có thể có nguy cơ cao hơn về các biến chứng COVID-19 và tử vong do cơn bão thượng thận, mặc dù điều này vẫn chưa được mô tả. Một số ý kiến gần đây cũng nhấn mạnh những rủi ro gia tăng đối mặt với những bệnh nhân dùng glucorticoids liều sinh lý và siêu sinh lý, đồng thời khuyến khích việc xác định những bệnh nhân này và tư vấn về những rủi ro có thể xảy ra và biện pháp phòng ngừa. Bệnh nhân mắc AI có nguy cơ lây nhiễm cao và những bệnh nhân mắc AI nguyên phát đã được chứng minh là đã giảm đáng kể độc tính tế bào NK do đó có thể ảnh hưởng đến việc nhận biết và loại bỏ sớm các tế bào bị nhiễm virus và làm suy giảm khả năng miễn dịch chống virus, mặc dù COVID-19 nguy cơ lây nhiễm cụ thể chưa được báo cáo cho đến nay. Gần đây, hướng dẫn cụ thể cho việc quản lý AI trong COVID-19 đã được xuất bản, đưa ra các quy tắc cụ thể trong ngày ốm ngoài việc củng cố tầm quan trọng của giáo dục và giãn cách xã hội. Hướng dẫn này khuyến cáo rằng người lớn mắc AI đang được điều trị bằng glucocorticoid liều sinh lý và COVID-19 cấp tính đang nghi ngờ hoặc đã được xác nhận nên tăng gấp đôi liều hydrocortisone buổi sáng của họ và sau đó uống 20mg hydrocortisone mỗi 6 giờ để cung cấp độ bao phủ glucocorticoid cách đều nhau đối với tình trạng viêm cấp tính dai dẳng và thường sốt liên tục ở bệnh nhân COVID-19. Những người dùng prendisonole 5–15 mg mỗi ngày nên dùng 10mg sau mỗi 12 giờ trong khi những người dùng liều prednisolone > 15 mg nên tiếp tục dùng liều prednisolone hàng ngày thông thường của họ nhưng nên chia nhỏ liều này thành liều buổi sáng và buổi chiều ít nhất 10mg mỗi lần. Một khi bệnh nhân hết sốt và cải thiện đáng kể về mặt lâm sàng, có thể giảm liều hydrocortisone để tăng gấp đôi liều thay thế sinh lý và sau đó là liều thông thường khi hồi phục hoàn toàn. Nếu các triệu chứng lâm sàng và dấu hiệu của COVID-19 xấu đi, bệnh nhân nên liên hệ với các dịch vụ y tế khẩn cấp và tiêm hydrocortisone 100 mg dưới da hoặc tiêm bắp (hoặc uống 50–100 mg hydrocortisone nếu không có thuốc tiêm này). Những người đồng mắc AI và COVID-19 và yêu cầu thở máy hoặc bị bệnh nặng, nên được dùng theo hướng dẫn về liều lượng do stress cấp tính ( bảng 2 ). Ngoài ra, việc dự phòng thuyên tắc huyết khối tĩnh mạch bằng heparin ở những bệnh nhân đang dùng glucocorticoid được khuyến cáo, do làm tăng nguy cơ huyết khối ở COVID-19. Hơn nữa, nguy cơ gia tăng đối với những người bị thiếu hụt thùy sau tuyến yên và các bất thường về điện giải đã được nghiên cứu một cách hợp lý và sự cần thiết phải dự trữ nguồn cung cấp hợp lý được nhấn mạnh.
Trong một phần khác, đề cập đến việc quản lý hội chứng Cushing trong đại dịch COVID-19, trì hoãn chẩn đoán sinh hóa đối với hội chứng Cushing nhẹ, quản lý thích hợp các bệnh đi kèm, đánh giá nguy cơ-lợi ích của điều trị dứt điểm (điều trị bằng thuốc và phẫu thuật) và dự phòng Pneumocystis jirovec i đã được nhấn mạnh. Theo các tác giả, đối với những người đang điều trị bằng thuốc, việc xác định liều thích hợp theo các đặc điểm lâm sàng hoặc trên cơ sở các giá trị sinh hóa gần đây nhất là hợp lý. Các tác giả cũng khuyên nên hoãn các nghiên cứu hình ảnh và khu trú cho các trường hợp nghi ngờ (nhẹ). Hơn nữa, họ khuyến nghị chỉ điều trị khẩn cấp trong các tình huống nguy hiểm đến tính mạng và thị giác và củng cố các quy tắc trong khi ốm, nhấn mạnh sự cần thiết phải đánh giá lại việc chăm sóc những bệnh nhân này sau khi đại dịch giảm bớt hoặc trong tầm kiểm soát ở khu vực địa phương.
Trục hạ đồi – tuyến yên – tuyến giáp
Được biết, các thụ thể ACE2 cũng được biểu hiện trong mô tuyến giáp và đóng một vai trò quan trọng trong các quá trình sinh lý. Một biểu hiện quá mức của ACE2 cũng liên quan đến sự tiến triển ung thư tuyến giáp. Ở động vật cường giáp, hoạt động của angiotensin 1-7 ở tim được tăng cường, cho thấy tác dụng điều hòa hệ thống renin-angiotensin-aldosterone của hormone tuyến giáp. Trong các nghiên cứu quan sát, các bất thường về tuyến giáp, bao gồm hội chứng bệnh lý bình giáp và viêm tuyến giáp, được báo cáo ở 3,6% bệnh nhân và các rối loạn nội tiết khác (trừ ĐTĐ và THA) có ở 13% bệnh nhân COVID-19. Tổn thương trực tiếp đến mô tuyến giáp do COVID-19 cũng đã được báo cáo khi khám nghiệm tử thi. Rối loạn tuyến giáp cũng có liên quan đến nguy cơ tử vong cao hơn trong một báo cáo. Từ quan điểm thực hành lâm sàng, việc quản lý bệnh tuyến giáp cấu trúc cần được xem xét cẩn thận. Đặc biệt, chúng tôi đồng ý với một ý kiến đề xuất ưu tiên điều trị nghi ngờ ung thư tuyến giáp thể tủy không biệt hóa và thể tiến triển (calcitonin ≥10 pg/ml huyết thanh) trong khi trì hoãn việc chăm sóc ung thư tuyến giáp biệt hóa ít tiến triển hơn.
Đái tháo nhạt
Đái tháo nhạt trung ương và đái tháo nhạt do thận (DI) đặt ra một thách thức đặc biệt do tính sẵn có của xét nghiệm điện giải (điện giải đồ) trong phòng thí nghiệm giảm. Một phần ý kiến gần đây đã nêu bật thách thức này, khuyến khích việc thực hành aquaresis mỗi tuần một lần bằng cách bỏ qua một liều vasopressin ở những người mắc DI. Điều này chủ yếu sẽ ngăn chặn việc giữ lại lượng nước tự do dư thừa và do đó duy trì tình trạng eunatremia. Hơn nữa, họ nhấn mạnh rằng nguy cơ chính ở những bệnh nhân này là hạ natri máu, có thể được giảm thiểu bằng cách đo trọng lượng cơ thể hàng ngày, tự nhận biết sớm các đặc điểm lâm sàng của hạ natri máu và tư vấn cho bệnh nhân uống để giải khát. Khi điều trị nội trú, bệnh nhân dễ bị hạ natri máu do điều trị quá mức DI, và thừa vasopressin do viêm phổi COVID-19 trong bối cảnh hội chứng tiết hormone chống bài niệu không thích hợp. Vì lý do đó, nước muối 0,9% nên được sử dụng để phục hồi thể tích và trong tình trạng bệnh nguy kịch khi mà trong tình trạng này hay xảy ra sự thay đổi thường xuyên trong phân phối thể tích. Hơn nữa, nên thường xuyên đánh giá lâm sàng và sinh hóa về tình trạng natri, dịch truyền nhược trương nên được chỉ định ở bệnh nhân tăng natri máu. Cần đặc biệt thận trọng trong việc chăm sóc bệnh nhân DI không uống nhiều và các chuyên gia tư vấn nội tiết nên sớm tham gia vào quá trình điều trị nội trú của bệnh nhân.
Chuyển hóa xương và khoáng chất
Mặc dù không có bằng chứng về việc tăng nguy cơ mắc COVID-19 đối với bệnh nhân bị rối loạn chuyển hóa xương – khoáng chất, nhưng các đợt giãn cách xã hội toàn cầu chưa từng có đã ảnh hưởng đáng kể đến việc chăm sóc bệnh nhân. Do hầu hết các trung tâm truyền dịch, phòng thí nghiệm ngoại trú và trung tâm quét xương tạm thời đóng cửa, Tổ chức Loãng xương Quốc gia đã đưa ra một tuyên bố hướng dẫn ( bảng 2 ). Những người đang dùng thuốc như Denosumab và Romosozumab được khuyến cáo nên được truyền dịch kịp thời, tuy nhiên, việc truyền bisphosphonat như acid zolendronic có thể bị hoãn lại do thời gian bán hủy của chúng dài.
Tăng lipid máu
Tăng lipid máu hiện diện ở 5% bệnh nhân theo một đánh giá trên 190 bệnh nhân nhập viện vì COVID-19. Sự phát triển của các bất thường về chuyển hóa / lipid ở những bệnh nhân hồi phục sau COVID-19 cũng có thể được dự đoán dựa trên dữ liệu từ nhóm thuần tập SARS. Các bác sĩ nội tiết có thể là nhà cung cấp dịch vụ chăm sóc sức khỏe cho nhóm này trong tương lai và nên cảnh giác với các biến chứng chuyển hóa lâu dài có thể tồn tại sau khi nhiễm COVID-19.
Một số báo cáo về tỷ lệ tử vong cao hơn ở người Da đen và gốc Tây Ban Nha đã xuất hiện. CDC gần đây đã báo cáo rằng 33% bệnh nhân nội trú COVID-19 ở Hoa Kỳ là người Da đen mặc dù chỉ chiếm 13% dân số Hoa Kỳ. Bang Louisiana báo cáo rằng bệnh nhân da đen và châu Á chiếm 59% và 0,83% trong số những người tử vong vì COVID-19. Thành phố New York cũng báo cáo tỷ lệ tử vong không tương xứng giữa người gốc Tây Ban Nha và người da đen. Mặc dù biểu hiện ACE2 cao hơn ở dân số châu Á so với người da trắng hoặc da đen, kiến thức hiện tại của chúng tôi về những khác biệt này không giải thích được cho tỷ lệ tử vong không cân xứng. Kết quả này có khả năng là do nhiều yếu tố: 1. Khuynh hướng di truyền cao hơn đối với rối loạn nội tiết, chẳng hạn như tỷ lệ THA gia tăng ở người da đen và béo phì ở bệnh nhân Latinh / Tây Ban Nha và 2. Sự không bình đẳng chủng tộc trong việc tiếp cận dịch vụ chăm sóc sức khỏe và bệnh viện có thể trì hoãn việc chăm sóc kịp thời, cùng với bệnh mãn tính tiềm ẩn được kiểm soát dưới mức tối ưu. Dữ liệu giám sát CDC về tỷ lệ nhập viện liên quan đến COVID-19 của bệnh nhân trong thời gian 4 tuần kết thúc vào ngày 28 tháng 3 năm 2020, là 4,6 trên 100.000 dân, với dữ liệu chủng tộc / dân tộc sau: 261 (45,0%) không phải Người da trắng gốc Tây Ban Nha (Da trắng), 192 (33,1%) là người da đen không phải gốc Tây Ban Nha (Da đen), 47 (8,1%) là người gốc Tây Ban Nha, 32 (5,5%) là người châu Á, hai (0,3%) là người Mỹ da đỏ / thổ dân Alaska và 46 (7,9%) thuộc chủng tộc khác hoặc không rõ. Những rào cản xã hội này đối với các nhóm thiểu số làm tăng khả năng dễ bị tổn thương của họ đối với bệnh nội tiết nói chung và hậu quả là đối với COVID-19.
Ở Mỹ, hơn một nửa số ca nhập viện liên quan đến COVID-19 xảy ra ở nam giới (5,1 so với 4,1 trên 100.000 dân). Sự khác biệt về giới tính đối với các bệnh nhiễm trùng nói chung có thể là do nhiều yếu tố, bao gồm mức độ mạnh mẽ của các phản ứng miễn dịch (cả bẩm sinh và thích nghi), sản xuất hormone steroid phụ thuộc vào giới tính (bao gồm testosterone và estrogen), các gen liên kết X liên quan đến phản ứng miễn dịch và sự hiện diện của các gene nhạy cảm với bệnh. Con đường truyền tín hiệu của thụ thể estrogen đã được xác định là rất quan trọng để bảo vệ ở phụ nữ bị nhiễm coronavirus. Một lời giải thích hợp lý cho tỷ lệ mắc COVID-19 cao hơn ở nam giới có thể liên quan đến các bước sau khi ACE2 gắn với SARS-CoV-2. Như đã mô tả trước đây, capsid của virus SARS-CoV-2 liên kết với ACE2 bề mặt và sau đó tương tác với protease serine của tế bào TMPRSS2 để mồi protein ( Hình 2 ). Từ các nghiên cứu về ung thư, người ta biết rằng TMPRSS2 là một gen đáp ứng androgen, được biểu hiện rất nhiều ở nam giới. Theo đề xuất của một nghiên cứu, sự biểu hiện TMPRSS2 cao hơn ở nam giới có thể là nguyên nhân khiến nam giới dễ bị tổn thương hơn đối với COVID-19. Cần có các nghiên cứu sâu hơn để xác định sự khác biệt về giới tính trong các kết quả liên quan đến COVID-19.
Nhiễm virus gây suy giảm miễn dịch ở người (HIV) và ung thư ở người chuyển giới có tỷ lệ cao hơn so với dân số chung. Những tình trạng này cùng với các bệnh nội tiết đã có từ trước có thể ảnh hưởng đến chức năng miễn dịch, có lẽ dẫn đến nguy cơ COVID-19 cao hơn ở những người chuyển giới. Tuy nhiên, hiện tại không có bằng chứng được công bố để hỗ trợ điều này. Người chuyển giới cũng thường xuyên phải đối mặt với những thách thức xã hội như nghèo đói, vô gia cư và không được tiếp cận với dịch vụ chăm sóc sức khỏe không đầy đủ, làm giảm khả năng tuân thủ các biện pháp phòng ngừa COVID-19 và tìm kiếm sự chăm sóc kịp thời. Do đó, các bác sĩ lâm sàng cần khuyến cáo và hướng dẫn cụ thể cho đối tượng này trong khi vẫn đảm bảo sử dụng đủ thuốc theo toa. Kế hoạch hành động có tại: https://transequality.org/covid19/plan ( bảng 2 ). Đối với các thủ thuật tự chọn như phẫu thuật xác nhận giới tính, việc hoãn lại là phù hợp theo hướng dẫn của CDC và WHO.
Kết luận, các bác sĩ nội tiết thường xuyên chăm sóc cho một tỷ lệ cao bệnh nhân dễ bị tổn thương bởi COVID-19, những người có nguy cơ cao bị các biến chứng đe dọa tính mạng. Bác sĩ lâm sàng nên tư vấn cho bệnh nhân về sự chuẩn bị cho trường hợp khẩn cấp, các kế hoạch dự phòng, duy trì nguồn cung cấp đầy đủ nhưng không quá mức, giãn cách xã hội và tiếp cận các nguồn thông tin đáng tin cậy. Hơn nữa, chỉ nên thận trọng dựa trên bằng chứng sẵn có và cần thận trọng đối với các quyết định dựa trên bằng chứng không đầy đủ hoặc không thuyết phục. Các biện pháp này có thể giảm thiểu một số rủi ro mà nhóm bệnh nhân dễ bị tổn thương của chúng ta phải đối mặt trong cuộc khủng hoảng chưa từng có này.
Theo kiến thức tốt nhất của các tác giả, các nghiên cứu trong bài báo này báo cáo dữ liệu từ các quần thể bệnh nhân khác nhau phù hợp với công bố khoa học đạo đức, một vấn đề đáng quan tâm trong thời gian gần đây 166 . Ngoài ra, do cuộc khủng hoảng COVID-19 đang diễn ra, tài liệu này không dựa trên đánh giá hệ thống rộng rãi hoặc phân tích tổng hợp, mà dựa trên sự đồng thuận của chuyên gia. Tài liệu chỉ nên được coi là hướng dẫn; nó không nhằm xác định một tiêu chuẩn chăm sóc y tế tuyệt đối. Các bác sĩ liên quan phải lập kế hoạch quản lý cho từng bệnh nhân
Tài liệu tham khảo:


